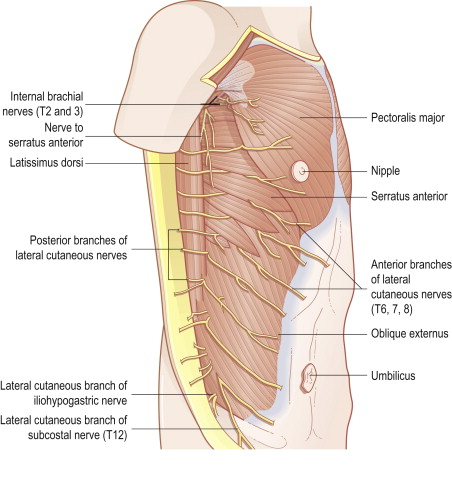
肩と腰の痛みあり。炎症反応高値
上腕二頭筋腱炎および肩周囲の滑液包炎あり。
PMR? late onset RA ?
さらにCPK高値、低左心機能で循環器でCAGするも正常範囲と。
エコーからは心筋炎も合併?
Cardiac Manifestations of Rheumatological Conditions: A Narrative Review
心血管疾患は、全身性のリウマチ性疾患において一般的に合併する。
診断時もしくは診断後に心血管性疾患を認めることがある。
さらに、心臓合併症がリウマチ疾患の最初の症状であることもありうるので、最初に心臓専門医が診ることもある。
心臓合併症は、無症候性から重症に変化しうるし、積極的な免疫抑制を必要としうる。
これらの合併症の診断は治療をするうえでも大切である。
リウマチ性疾患では動脈硬化や虚血性心疾患のリスクも上がり、死亡率上昇の原因となりうる。
炎症の積極的なコントロールは、心血管疾患、特に虚血性心疾患のリスクを低下させる。
ただ、はっきりとしたガイドラインやリコメンデーションは存在していない。
以下、心血管性合併症をおこす代表的なリウマチ性疾患
①関節リウマチ
②SLE
③全身性強皮症
④強直性脊椎炎
⑥乾癬性関節炎
⑦多発筋炎・皮膚筋炎
⑧高安血管炎
⑨GCA
⑩PAN
⑪チャーグストラウス
⑫ベーチェット
⇒PMRの記載はなく、PMRの心病変はあまり一般的ではないのかもしれない。

リウマチ性疾患と心血管合併症の対応図
Int J Cardiol. 2017 Jun 1;236:151-156. doi: 10.1016/j.ijcard.2017.01.104. Epub 2017 Feb 1.
膠原病(connective tissue disorder⇒CTD)の心病変をMRIで評価した study(cardio-vascular magnetic resonance を評価⇒CMR)
CMRを心臓病変を伴わない未治療のCTD78例で評価(年齢43歳、女性59 /男性 19)
結果:高安の3/5、チャーグストラウスの3/4 、ウェゲナーの4/5 、SLEの10/16、関節リウマチの9/12 RA、混合性結合組織病の6/8 、強直性脊椎炎の4/12 AS、リウマチ性多発筋痛症の1/3 PMR、全身性強皮症の2/8、皮膚筋炎の2 /5 でMRIのT2比は正常と比較して高かった(2.78±0.25対1.5±0.2、p <0.01)
心筋炎は、1人のTA、1人のSLE、1人のRA、1人のSScおよび2人のDM患者において同定。
びまん性の内膜下線維化は1人のCSS、1人のRA患者で同定
内膜下の心虚血は3人のSLE、1人のMCTD、1人のMCTD,2人のRADで同定
心筋炎は、1人のTA、1人のSLE、1人のRA、1人のSScおよび2人のDM患者において同定された。
リウマチ性疾患を治療したところ、6および12ヵ月後のCMR再評価でT2比の有意な改善を認めることより、心病変は免疫抑制で改善しうる。
PMRにおけるステロイド使用者で心血管イベントが増えるか検討したstudy

⇒PMRにおいてステロイド使用は心血管イベント増加につながらない。
では、PMRで心筋炎をきたしうるのか??
PMRで心筋炎をきたしたケースレポート。
Myocardial inflammation in polymyalgia rheumatica assessed using cardiac magnetic resonance imaging
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3718596/
PMRとしてステロイドテーパリング中に頻脈を認めたところ、エコーでEF40%に低下していたのでMRIで精査をした。

MRIではやはり心筋のT2比が増加しており、心筋浮腫が示唆される。
ACE-Iとβblockerの導入で心筋症は改善したと。
報告は限られているが、PMRは心筋炎をきたしうる。
また、ACE-Iとβblocker±免疫抑制療法で症状は改善するかもしれない